Quirónsalud
Blog del Servicio de Hematología de la Fundación Jiménez Díaz
- 202318dic
Cómo evitar la “trombosis del viajero” y recomendaciones para viajeros que toman anticoagulantes
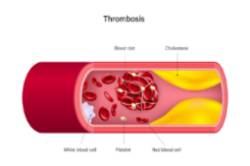
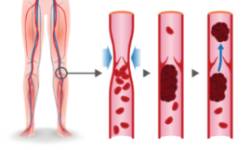
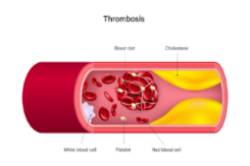
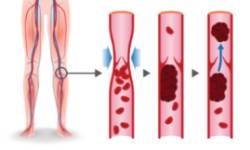
La trombosis del viajero, antes llamada "síndrome de la clase turista" consiste en la formación de un coágulo en las venas de las piernas. Existe el riesgo de que ese coágulo se desprenda y pueda llegar a la circulación pulmonar provocando una embolia de pulmón. Esta complicación puede asociarse con viajes de duración superior a 4 horas, si bien el riesgo de trombosis aumenta aún más en viajes de más de 8 horas.
Aunque inicialmente la trombosis del viajero se describió en personas que viajaban en avión, este riesgo existe también en desplazamientos en coche, autobús u otro medio de transporte que obligue a reducir mucho la movilidad de las piernas. Se conoce que un viaje prolongado multiplica por 2 o 3 el riesgo de trombosis venosa.
Por otro lado, hay pacientes que están recibiendo medicación anticoagulante de forma habitual, y que deben tomar ciertas precauciones antes de iniciar un viaje de larga duración.
En este artículo proponemos unas recomendaciones para conseguir que todos los viajeros, tengan o no factores de riesgo trombótico; o tomen un anticoagulante, se encuentren lo más seguros posibles en sus diferentes destinos.
¿Solo influye la falta de movilidad de las piernas en el desarrollo de la trombosis del viajero o contribuyen otros factores?
Cuando ocurre una trombosis venosa, la mayoría de las veces suelen concurrir varios factores, por ello decimos que la trombosis es multifactorial. Durante el viaje, el mantener una misma postura de forma muy prolongada, hace que se pueda enlentecer la circulación sanguínea en las piernas y en ocasiones, activarse el sistema de la coagulación. Sin embargo, esta inmovilización no es la única causa, ya que hay que tener en cuenta otros factores, presentes en el viajero, que "ayudan" a que aumente el riesgo trombótico.
En blog anteriores, hemos hablado de los factores de riesgo generales de la trombosis venosa. La edad avanzada, el tabaquismo, la obesidad y la gestación conllevan un mayor riesgo trombótico, así como tomar determinados fármacos como los anticonceptivos hormonales combinados, o tener alguna enfermedad, tal es el caso del cáncer, haber tenido un traumatismo o una cirugía reciente, etcétera. A los factores anteriores hay que unir condiciones genéticas (trombofilia hereditaria) o adquiridas que se asocian a una hipercoagulabilidad de la sangre.
¿Podemos prevenir el desarrollo de la trombosis del viajero?
En líneas generales, cuando se va a realizar un viaje de larga duración, se aconseja mantener una hidratación adecuada, mantener activa la circulación de las piernas, bien dando paseos durante el viaje (en caso de transporte por tierra, se aconsejar para y dar un paseo cada 2 horas), haciendo movimientos de flexo-extensión de las piernas, sin olvidarnos del pie. ¡Por supuesto evitar llevar ropas ajustadas!
A estos consejos generales, en ocasiones hay que unir otras medidas como las medias de compresión e incluso en pacientes con riesgo trombótico elevado, que acuda a su médico para valorar si tiene que usar algún fármaco anticoagulante (enlentece la circulación sanguínea, por ejemplo, la heparina) antes de iniciar el viaje.
¿Cómo puedo detectar que estoy teniendo una trombosis en las piernas?
Los signos y síntomas a veces pueden pasar desapercibidos o confundirlos, por ejemplo, con una contractura muscular. Suele aparecer con mayor frecuencia, edema y enrojecimiento de la pierna y dolor en alguna parte de esta. Si tenemos estos síntomas, tan pronto podamos, debe evaluarnos un médico y plantear hacer una ecografía doppler.
Hay que tener en cuenta que los síntomas de la trombosis pueden aparecer inmediatamente después del viaje e incluso presentarse varias semanas después.
¿Puedo hacer un viaje si estoy tomando un fármaco anticoagulante?
En ocasiones, la persona que va a viajar ya ha tenido una trombosis y está recibiendo tratamiento anticoagulante. No existe ninguna contraindicación para realizar viajes largos o coger vuelos con el tratamiento anticoagulante, ya sea con fármacos antagonistas de la vitamina K (acenocumarol o warfarina), anticoagulantes orales de acción directa (edoxabán, rivaroxabán, apiixabán o dabigatrán) o con heparina de bajo peso molecular. Se debe continuar con su dosis de tratamiento habitual sin realizar cambios.
Por otro lado, entre los anticoagulantes mencionados, los que presentan mayor variabilidad de dosificación y necesitan de un control periódico más estricto son los antagonistas de la vitamina K, el más conocido el Sintrom®. Su monitorización del efecto anticoagulante se realiza a través del parámetro conocido como INR. Si una persona se encuentra en tratamiento con esta medicación y va a realizar un viaje prolongado, debería estar en un rango de INR lo más estable posible para evitar complicaciones trombóticas o hemorrágicas.
Para ello, debe acudir al médico que realiza habitualmente el control de su tratamiento anticoagulante previo a iniciar el viaje y establecer un intervalo temporal de medición de INR adecuado. Se debe tener en cuenta el tiempo que va a estar "fuera" y especificar la necesidad de realizar mediciones del INR durante el viaje, para poder establecer un adecuado método de control en el lugar de destino. Además, la persona anticoagulada debe estar familiarizada con el proceder en casos de ocurrir alguna complicación. En estas ocasiones, los programas de autocontrol o de telecontrol, suponen una ventaja al paciente, al poder realizarse la automedición del INR mediante punción capilar en un coagulómetro portátil, y ajustar él mismo la dosis o remitirle a su médico el resultado del INR para recibir, posteriormente la dosificación del fármaco.
Si se encuentra en tratamiento con antagonistas de la vitamina K, debe tener especial precaución con la alimentación y las enfermedades gastrointestinales. Estos anticoagulantes actúan inhibiendo los factores de la coagulación dependientes de vitamina K que se absorbe de los alimentos, por lo que un cambio en la dieta o una gastroenteritis (cambios en la cantidad de absorción de vitamina K) pueden afectar a los niveles de INR. En caso de gastroenteritis intensa se recomienda ponerse en contacto con un centro sanitario para valorar la necesidad de realizar el ajuste necesario sobre esta medicación.
Recomendaciones generales del "viajero"
Toda persona que vaya a viajar debe seguir las recomendaciones habituales de los viajeros, teniendo además en cuenta su afección médica, junto con su gravedad y tratamiento.
La principal recomendación ante un viaje planificado es acudir a su médico tratante de su trastorno de la coagulación para que pueda evaluar la idoneidad de su viaje y realizar recomendaciones individualizadas teniendo en cuenta la relevancia de su afección en dicho contexto.
Se recomienda también estudiar la calidad de la atención sanitaria en el país/lugar de destino recabando información sobre la calidad de su servicio sanitario, la posibilidad de recibir medicación en dicho país o la incidencia de enfermedades o epidemias que puedan tener lugar en el momento del viaje. Para ello se recomienda el uso de la página de recomendaciones de viaje del Ministerio de Asuntos Exteriores, Unión Europea y Cooperación de España (https://www.exteriores.gob.es/es/ServiciosAlCiudadano/Paginas/Recomendaciones-de-viaje.aspx
 ) donde tienen un apartado específico sobre salud y se pueden encontrar los principales centros médicos u hospitales de referencia. Más concretamente, las personas diagnosticadas de hemofilia pueden consultar en la página de la Federación Mundial de Hemofilia (FMH) donde encontrarán un documento con los centros especializados en dicha patología de cada país (https://wfh.org/es/encuentre-apoyo-local/#tips
) donde tienen un apartado específico sobre salud y se pueden encontrar los principales centros médicos u hospitales de referencia. Más concretamente, las personas diagnosticadas de hemofilia pueden consultar en la página de la Federación Mundial de Hemofilia (FMH) donde encontrarán un documento con los centros especializados en dicha patología de cada país (https://wfh.org/es/encuentre-apoyo-local/#tips ).
).En afecciones graves, sería recomendable, además, llevar un informe más completo del médico sobre tipo de enfermedad y grado de afección.
En cuanto a su medicación habitual, se recomienda llevar la medicación necesaria para cubrir su estancia durante el viaje. Es importante llevar la medicación como equipaje de mano y "NO" en la bodega porque los cambios de temperatura pueden afectar a los principios químicos de su medicación y tiene más facilidad para sufrir algún contratiempo como romperse o perderse. Se debe consultar también las restricciones de entrada de medicamentos en el país de destino, así como las normativas de medicamentos de las distintas compañías aéreas.
Es recomendable contratar un seguro integral de viaje, tratando de incluir las posibles complicaciones habituales de la patología subyacente, así como los riesgos derivados de las actividades que se realizarán en el destino.
Siga las recomendaciones comentadas "al pie de la letra" y ¡buen viaje sin complicaciones!
Enlaces de interés:
Recomendaciones del Ministerio de Sanidad: https://www.sanidad.gob.es/areas/sanidadExterior/laSaludTambienViaja/consejosSanitarios/consejosViajero.htm

Recomendaciones del Ministerio de Asuntos Exteriores: https://www.exteriores.gob.es/es/ServiciosAlCiudadano/Paginas/Recomendaciones-de-viaje.aspx

Recomendaciones en trastornos de la coagulación del NaHTNaC: https://travelhealthpro.org.uk/factsheet/107/coagulation-disorders

Dr. Raúl Pérez Calle
- 20236nov
Descubriendo los eosinófilos, desconocidos guardianes de la inmunidad
En lo más profundo de nuestro sistema inmunológico existen héroes silenciosos que desempeñan un papel crucial en la protección de nuestro cuerpo contra las amenazas externas. Los eosinófilos son uno de estos valientes defensores. Aunque menos afamados que otros componentes del sistema inmune, como los linfocitos, los eosinófilos ejercen un importante papel en el mantenimiento de nuestra salud a través de diferentes mecanismos.
¿Qué son los eosinófilos?
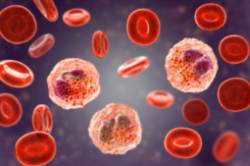
Tal y como se comentaba previamente, se tratan de un tipo de glóbulo blanco, o como solemos llamarlos, "leucocitos", por lo que forman parte de las líneas de protección de nuestro organismo. Son células con un núcleo bilobulado y con un citoplasma lleno de gránulos que se tiñen de forma característica. Esto es precisamente lo que da su nombre a los eosinófilos, término que proviene del griego eos- "amanecer, aurora (color rosado)", y -philos, "aficionado a, con preferencia por". Y es que, cuando examinamos la sangre al microscopio en lo que llamamos frotis (que no es más que una gota de ella extendida en un cristal y teñida con colorantes específicos), vemos estas células rosadas, anaranjadas.
¿Qué funciones realizan en el cuerpo?
La principal función y más ancestral de los eosinófilos es defender al organismo de las infecciones parasitarias o infestaciones. Los parásitos son seres vivos que pueden ser unicelulares, como los protozoos o las amebas, o por el contrario pluricelulares (tenias o cestodos, nematodos y un largo etcétera) y que, como característica fundamental, precisan de otro ser vivo para poder realizar todas o algunas de sus funciones vitales, del que dependen y al que generalmente ocasionan algún tipo de perjuicio durante su ciclo vital.
Los eosinófilos poseen sustancias en sus gránulos que al ser liberadas atacan a estos invasores para destruirlos, y que de proliferar serían capaces de producir multitud de enfermedades, como es el caso de la malaria, la enfermedad del sueño o la oxiuriasis o infestación por lombrices intestinales. Si bien es cierto que son enfermedades a priori poco habituales en nuestro medio, y que eran más frecuentes hace años, cuando las condiciones higiénicas eran peores, la globalización y la frecuencia de viajes y el turismo a áreas menos favorecidas precisan de su control.
Además, juegan también un importante papel en el control de las reacciones alérgicas o de hipersensibilidad, sobre las que posteriormente hablaremos.
¿Tengo que preocuparme si veo que tengo los eosinófilos bajos en una analítica? ¿Y si salen altos? ¿Qué es la eosinofilia?
Aunque las cifras normales de los diferentes tipos de células en la sangre pueden variar ligeramente en función del laboratorio, consideramos que el rango habitual para los eosinófilos oscila entre 0,0 y 0,5 células por mm3. Sí, tal y como habéis leído, encontrar 0 eosinófilos en un análisis de sangre no supone ningún problema. Y es que estas células mantienen unos niveles tremendamente oscilantes y que se ven sujetos a multitud de factores externos. Por ejemplo, son "células nocturnas", por lo que, si realizamos un estudio durante el final de la tarde o la medianoche, el número será mucho más elevado que si lo hacemos a primera hora de la mañana. Es por esto que no se considera que la "eosinopenia", es decir, una cifra baja de eosinófilos en sangre sea una condición patológica.
En el caso de que observemos un número elevado, lo primero que haremos será repetir la analítica a posteriori para confirmar el resultado. Hablamos de eosinofilia cuando observamos niveles mantenidos y superiores a 0,5 células por mm3, pudiendo ser dividida a su vez en leve (hasta 1,5 células por mm3), moderada (1,5-5,0 células por mm3) y grave (>5,0 células por mm3).
¿Hay enfermedades que se relacionan con trastornos que afecten a los eosinófilos?
Múltiples circunstancias pueden ocasionar una elevación en el número de eosinófilos en sangre. En primer lugar, debe valorarse si esta elevación se trata de un hallazgo aislado o si por el contrario es mantenida y si se acompaña de síntomas. Los pacientes con eosinofilia pueden encontrarse asintomáticos o presentar multitud de manifestaciones clínicas, que abarcan desde lesiones en la piel o episodios de tos y falta de aire, a otras complicaciones que pueden llegar a comprometer la vida. En función de estos datos se excluirán las múltiples causas secundarias (fundamentalmente infecciosas o autoinmunes) que pueden ocasionar eosinofilia.
Si no se demuestra ninguna otra etiología, es aconsejable estudiar la eosinofilia de forma más detallada en el Servicio de Hematología, pues existen entidades, de naturaleza clonal y generalmente crónica (aunque en ocasiones maligna), que a pesar de ser bastante infrecuentes pueden elevar el número de eosinófilos. En estos casos será el hematólogo el que determinará que estudios se realizarán, ya sean en sangre periférica o incluso en la médula ósea (la "fábrica" y origen de todas las células de la sangre).
Si previamente ya mencionamos las infecciones parasitarias, no podemos olvidarnos del otro gran pilar en el que intervienen los eosinófilos, que son las reacciones alérgicas y de hipersensibilidad, así como el conocido asma, con idéntico mecanismo.
¿Qué es la hipersensibilidad?
Llamamos hipersensibilidad a la situación en la cual se observa una reacción inmunitaria exagerada ante un aloantígeno, es decir, una sustancia extraña al organismo y que provoca una respuesta inmune generando anticuerpos. Para que puedan tener lugar las reacciones de hipersensibilidad se precisa de una sensibilización previa, es decir, haber tenido contacto con esta "sustancia extraña". Y os preguntaréis, ¿por qué? Existen 4 tipos de hipersensibilidad, siendo el tipo I la más relevante (y en la que nos centraremos ahora), la que se relaciona con los eosinófilos y que es inmediata y mediada por un tipo de anticuerpo (proteínas que nos defienden y que son producidas por otro tipo de glóbulo blanco, los linfocitos B) que se conoce como inmunoglobulina E.
Cuando una persona se expone a alguna sustancia que ocasiona que su sistema inmune reaccione de forma exagerada (en la mayoría de las personas esta reacción no tendría lugar, sino que simplemente se toleraría), ya se trate de algún alimento, planta, epitelio de animal o de ácaros, libera inmunoglobulinas E de forma no controlada. Estos anticuerpos se unirán a receptores específicos que poseen los eosinófilos y sus "hermanos mayores", los mastocitos, y se quedarán a la espera, dormidos. La próxima vez que dicha persona tenga contacto con la mencionada sustancia, la unión de esta a los anticuerpos inducirá la liberación de multitud de mediadores en estas células con importante actividad química, como son la histamina, los leucotrienos o las prostaglandinas, con efectos sobre el músculo liso o los epitelios. Esto provoca a su vez una reacción que puede ser localizada y limitada a un órgano, local aumentada (cuando es mayor de lo que se esperaría en un paciente alérgico) o anafiláctica cuando es desmedida y puede poner en riesgo la vida del paciente.
Por tanto, podemos concluir que uno se hace alérgico a lo que se expone. De acuerdo a esto, si tomo melocotón, una de mis frutas favoritas en verano, y decido un día acompañarlo de papaya por primera vez y se me inflaman los labios y la lengua, lo lógico es pensar que el causante habrá sido el melocotón, y no la papaya, ya que es la primera vez que nos exponemos a ella. Sería simplista plantear que las reacciones inmunológicas tienen lugar de forma tan directa, puesto que son algo mucho más complejo y existen diferentes interacciones entre alérgenos, si bien es cierto que valdría como primera aproximación.
En cuanto al tratamiento, lo que se suele hacer es emplear fármacos que antagonizan o bloquean los receptores de las sustancias que han liberado eosinófilos y mastocitos: antihistamínicos, corticoides, y en los casos en los que la reacción de hipersensibilidad amenaza la vida, adrenalina.
Esperemos que, después de estas líneas, hayamos aportado claridad a lo que son los eosinófilos, por qué son importantes como parte de nuestro sistema inmune, y la importancia de un correcto control de sus mecanismos de activación para evitar reacciones no deseadas. Pensad en ellos la próxima vez que estornudéis en primavera o si os vais de viaje a Tailandia.
Dr. Gonzalo Castellanos Arias
Servicio de Hematología
Hospital Universitario Fundación Jiménez Díaz
17 comentarios - 202313oct
Cómo evitar la “trombosis del viajero” y recomendaciones para viajeros que toman anticoagulantes
La trombosis del viajero, antes llamada "síndrome de la clase turista" consiste en la formación de un coágulo en las venas de las piernas. Existe el riesgo de que ese coágulo se desprenda y pueda llegar a la circulación pulmonar provocando una embolia de pulmón. Esta complicación puede asociarse con viajes de duración superior a 4 horas, si bien el riesgo de trombosis aumenta aún más en viajes de más de 8 horas.
Aunque inicialmente la trombosis del viajero se describió en personas que viajaban en avión, este riesgo existe también en desplazamientos en coche, autobús u otro medio de transporte que obligue a reducir mucho la movilidad de las piernas. Se conoce que un viaje prolongado multiplica por 2 o 3 el riesgo de trombosis venosa.
Por otro lado, hay pacientes que están recibiendo medicación anticoagulante de forma habitual, y que deben tomar ciertas precauciones antes de iniciar un viaje de larga duración.
En este artículo proponemos unas recomendaciones para conseguir que todos los viajeros, tengan o no factores de riesgo trombótico; o tomen un anticoagulante, se encuentren lo más seguros posibles en sus diferentes destinos.
¿Solo influye la falta de movilidad de las piernas en el desarrollo de la trombosis del viajero o contribuyen otros factores?
Cuando ocurre una trombosis venosa, la mayoría de las veces suelen concurrir varios factores, por ello decimos que la trombosis es multifactorial. Durante el viaje, el mantener una misma postura de forma muy prolongada, hace que se pueda enlentecer la circulación sanguínea en las piernas y en ocasiones, activarse el sistema de la coagulación. Sin embargo, esta inmovilización no es la única causa, ya que hay que tener en cuenta otros factores, presentes en el viajero, que "ayudan" a que aumente el riesgo trombótico.
En blog anteriores, hemos hablado de los factores de riesgo generales de la trombosis venosa. La edad avanzada, el tabaquismo, la obesidad y la gestación conllevan un mayor riesgo trombótico, así como tomar determinados fármacos como los anticonceptivos hormonales combinados, o tener alguna enfermedad, tal es el caso del cáncer, haber tenido un traumatismo o una cirugía reciente, etcétera. A los factores anteriores hay que unir condiciones genéticas (trombofilia hereditaria) o adquiridas que se asocian a una hipercoagulabilidad de la sangre.
¿Podemos prevenir el desarrollo de la trombosis del viajero?
En líneas generales, cuando se va a realizar un viaje de larga duración, se aconseja mantener una hidratación adecuada, mantener activa la circulación de las piernas, bien dando paseos durante el viaje (en caso de transporte por tierra, se aconsejar para y dar un paseo cada 2 horas), haciendo movimientos de flexo-extensión de las piernas, sin olvidarnos del pie. ¡Por supuesto evitar llevar ropas ajustadas!
A estos consejos generales, en ocasiones hay que unir otras medidas como las medias de compresión e incluso en pacientes con riesgo trombótico elevado, que acuda a su médico para valorar si tiene que usar algún fármaco anticoagulante (enlentece la circulación sanguínea, por ejemplo, la heparina) antes de iniciar el viaje.
¿Cómo puedo detectar que estoy teniendo una trombosis en las piernas?
Los signos y síntomas a veces pueden pasar desapercibidos o confundirlos, por ejemplo, con una contractura muscular. Suele aparecer con mayor frecuencia, edema y enrojecimiento de la pierna y dolor en alguna parte de esta. Si tenemos estos síntomas, tan pronto podamos, debe evaluarnos un médico y plantear hacer una ecografía doppler.
Hay que tener en cuenta que los síntomas de la trombosis pueden aparecer inmediatamente después del viaje e incluso presentarse varias semanas después.
¿Puedo hacer un viaje si estoy tomando un fármaco anticoagulante?
En ocasiones, la persona que va a viajar ya ha tenido una trombosis y está recibiendo tratamiento anticoagulante. No existe ninguna contraindicación para realizar viajes largos o coger vuelos con el tratamiento anticoagulante, ya sea con fármacos antagonistas de la vitamina K (acenocumarol o warfarina), anticoagulantes orales de acción directa (edoxabán, rivaroxabán, apiixabán o dabigatrán) o con heparina de bajo peso molecular. Se debe continuar con su dosis de tratamiento habitual sin realizar cambios.
Por otro lado, entre los anticoagulantes mencionados, los que presentan mayor variabilidad de dosificación y necesitan de un control periódico más estricto son los antagonistas de la vitamina K, el más conocido el Sintrom®. Su monitorización del efecto anticoagulante se realiza a través del parámetro conocido como INR. Si una persona se encuentra en tratamiento con esta medicación y va a realizar un viaje prolongado, debería estar en un rango de INR lo más estable posible para evitar complicaciones trombóticas o hemorrágicas.
Para ello, debe acudir al médico que realiza habitualmente el control de su tratamiento anticoagulante previo a iniciar el viaje y establecer un intervalo temporal de medición de INR adecuado. Se debe tener en cuenta el tiempo que va a estar "fuera" y especificar la necesidad de realizar mediciones del INR durante el viaje, para poder establecer un adecuado método de control en el lugar de destino. Además, la persona anticoagulada debe estar familiarizada con el proceder en casos de ocurrir alguna complicación. En estas ocasiones, los programas de autocontrol o de telecontrol, suponen una ventaja al paciente, al poder realizarse la automedición del INR mediante punción capilar en un coagulómetro portátil, y ajustar él mismo la dosis o remitirle a su médico el resultado del INR para recibir, posteriormente la dosificación del fármaco.
Si se encuentra en tratamiento con antagonistas de la vitamina K, debe tener especial precaución con la alimentación y las enfermedades gastrointestinales. Estos anticoagulantes actúan inhibiendo los factores de la coagulación dependientes de vitamina K que se absorbe de los alimentos, por lo que un cambio en la dieta o una gastroenteritis (cambios en la cantidad de absorción de vitamina K) pueden afectar a los niveles de INR. En caso de gastroenteritis intensa se recomienda ponerse en contacto con un centro sanitario para valorar la necesidad de realizar el ajuste necesario sobre esta medicación.
Recomendaciones generales del "viajero"
Toda persona que vaya a viajar debe seguir las recomendaciones habituales de los viajeros, teniendo además en cuenta su afección médica, junto con su gravedad y tratamiento.
La principal recomendación ante un viaje planificado es acudir a su médico tratante de su trastorno de la coagulación para que pueda evaluar la idoneidad de su viaje y realizar recomendaciones individualizadas teniendo en cuenta la relevancia de su afección en dicho contexto.
Se recomienda también estudiar la calidad de la atención sanitaria en el país/lugar de destino recabando información sobre la calidad de su servicio sanitario, la posibilidad de recibir medicación en dicho país o la incidencia de enfermedades o epidemias que puedan tener lugar en el momento del viaje. Para ello se recomienda el uso de la página de recomendaciones de viaje del Ministerio de Asuntos Exteriores, Unión Europea y Cooperación de España (https://www.exteriores.gob.es/es/ServiciosAlCiudadano/Paginas/Recomendaciones-de-viaje.aspx
 ) donde tienen un apartado específico sobre salud y se pueden encontrar los principales centros médicos u hospitales de referencia. Más concretamente, las personas diagnosticadas de hemofilia pueden consultar en la página de la Federación Mundial de Hemofilia (FMH) donde encontrarán un documento con los centros especializados en dicha patología de cada país (https://wfh.org/es/encuentre-apoyo-local/#tips
) donde tienen un apartado específico sobre salud y se pueden encontrar los principales centros médicos u hospitales de referencia. Más concretamente, las personas diagnosticadas de hemofilia pueden consultar en la página de la Federación Mundial de Hemofilia (FMH) donde encontrarán un documento con los centros especializados en dicha patología de cada país (https://wfh.org/es/encuentre-apoyo-local/#tips ).
).En afecciones graves, sería recomendable, además, llevar un informe más completo del médico sobre tipo de enfermedad y grado de afección.
En cuanto a su medicación habitual, se recomienda llevar la medicación necesaria para cubrir su estancia durante el viaje. Es importante llevar la medicación como equipaje de mano y "NO" en la bodega porque los cambios de temperatura pueden afectar a los principios químicos de su medicación y tiene más facilidad para sufrir algún contratiempo como romperse o perderse. Se debe consultar también las restricciones de entrada de medicamentos en el país de destino, así como las normativas de medicamentos de las distintas compañías aéreas.
Es recomendable contratar un seguro integral de viaje, tratando de incluir las posibles complicaciones habituales de la patología subyacente, así como los riesgos derivados de las actividades que se realizarán en el destino.
Siga las recomendaciones comentadas "al pie de la letra" y ¡buen viaje sin complicaciones!
Dr. Raúl Pérez Calle
Servicio de Hematología y Hemoterapia
Hospital Universitario Fundación Jiménez Díaz
Enlaces de interés:
- Recomendaciones del Ministerio de Sanidad: https://www.sanidad.gob.es/areas/sanidadExterior/laSaludTambienViaja/consejosSanitarios/consejosViajero.htm

- Recomendaciones del Ministerio de Asuntos Exteriores: https://www.exteriores.gob.es/es/ServiciosAlCiudadano/Paginas/Recomendaciones-de-viaje.aspx

- Recomendaciones en trastornos de la coagulación del NaHTNaC: https://travelhealthpro.org.uk/factsheet/107/coagulation-disorders

- Recomendaciones del Ministerio de Sanidad: https://www.sanidad.gob.es/areas/sanidadExterior/laSaludTambienViaja/consejosSanitarios/consejosViajero.htm
- 202313sep
Púrpura trombótica trombocitopénica, una enfermedad rara que requiere un diagnóstico y un tratamiento precoz
La púrpura trombótica trombocitopénica (PTT) es un trastorno de la sangre que se caracteriza por anemia hemolítica microangiopática y trombocitopenia, junto con otros hallazgos clínicos y de laboratorio que se comentarán más adelante. La anemia "hemolítica microangiopática" se llama así porque los glóbulos rojos se fragmentan y se destruyen en su tránsito por la sangre, debido a que sufren un traumatismo mecánico en los pequeños vasos sanguíneos. Es el caso de la anemia hemolítica en los corredores de maratón, en la que los glóbulos rojos sufren del impacto del pie en el suelo y los glóbulos rojos pueden fragmentarse. En la PTT el traumatismo lo produce la formación de coágulos de sangre en los pequeños vasos sanguíneos que hace que el flujo sanguíneo sea más turbulento.
La PTT una enfermedad rara, en España se diagnostican alrededor de 200 episodios al año, siendo más frecuente en mujeres con una edad media de diagnóstico en torno a los 40 años. El 95% de los casos son adquiridos o espontáneos y solo un 5% se producen por alteraciones congénitas. Además, al menos un 40% de los pacientes que sufren un episodio de PTT presentan una recaída.
La PTT es una enfermedad hematológica que se encuadra dentro de los síndromes denominados microangiopatías trombóticas (MAT). Las MAT se caracterizan por la presencia de unos anticuerpos que atacan una proteína llamada ADAMTS 13. Esta proteína la tenemos todos en nuestra sangre y es fundamental para regular el proceso de la coagulación sanguínea. Como se ha hablado en otro blog, cuando tiene lugar un daño vascular juega un papel muy importante el factor von Willebrand. Para poder ejercer su función hemostática debe producirse un cambio en su estructura gracias a la proteína ADAMTS 13.
La ausencia de ADAMTS 13 en el plasma produce un "factor von Willebrand alterado" que tiene más capacidad de unirse a las plaquetas, con el consiguiente aumento de la formación de trombos en los vasos pequeños del organismo. Esto trae como consecuencia que la sangre no llega a irrigar órganos importantes como son el cerebro, el riñón o el corazón. En los microtrombos se van acumulando plaquetas y todo ello ocasiona un flujo turbulento de la circulación sanguínea, provocando la rotura de los glóbulos rojos. Todas estas alteraciones producen la triada característica de esta enfermedad: anemia (descenso del número de glóbulos rojos funcionales y por tanto de la hemoglobina que éstos transportan), presencia de esquistocitos (fragmentos de glóbulos rojos en la circulación; viene de la palabra "esquisto" que significa "dividir") y trombocitopenia (descenso de plaquetas).
Clínicamente los pacientes presentan síntomas por la oclusión de los vasos, como son: cefalea, alteraciones visuales, en ocasiones obnubilación o cambios en el comportamiento, convulsiones o ictus. Pueden presentar molestias urinarias, con una orina de color rojizo. En ocasiones presentan náuseas o vómitos con dolor abdominal. La anemia suele provocar una sensación de cansancio, que suele aparecer de forma más o menos brusca. La trombocitopenia se asocia con lesiones cutáneas conocidas como "petequias" o "equímosis" (pequeños hematomas o manchitas rojizas localizadas por todo el cuerpo), acompañado de sangrados a distintos niveles, la nariz, el tubo digestivo, sangrados ginecológicos o incluso sangrados intracraneales.
Todos estos síntomas pueden aparecer en otros cuadros, ya que no son específicos de esta enfermedad, por eso es importante la sospecha clínica y el estudio de laboratorio.
En la analítica de un paciente con PTT solemos encontrar un descenso de la hemoglobina y de las plaquetas. La rotura de los hematíes en el interior de los vasos hace que aumente la bilirrubina y una enzima llamada lactato deshidrogenasa (LDH). Los tiempos de coagulación suelen ser normales. Además, al mirar al microscopio la extensión de sangre, se observan hematíes fragmentados y disminución de plaquetas. En la orina se ven restos de hematíes y en algunas ocasiones se detecta fallo del riñón e insuficiencia renal.
El diagnóstico definitivo se hace descartando otras causas que puedan cursar con los datos de laboratorio y clínicos con los que debuta la PTT. Sin embargo, para confirmar el diagnóstico es necesaria la determinación de la enzima ADAMTS 13, que resulta ser inferior al 10%.
Se debe iniciar el tratamiento sólo con la sospecha clínica y de laboratorio de este cuadro, ya que el inicio precoz mejora mucho la supervivencia. El tratamiento tiene dos objetivos: el primero de ellos, es eliminar los anticuerpos ya formados presentes en el plasma; y el segundo es disminuir o frenar la producción de dichos anticuerpos.
Para la eliminación de los anticuerpos ya formados se realiza un procedimiento que se denomina "recambio plasmático", en el que, a través de un procedimiento de aféresis, se elimina plasma del paciente que contiene los anticuerpos que están haciendo daño y se sustituye por plasma de un donante sano, que contiene la enzima ADAMTS 13, deficitaria en el paciente. Para frenar la producción de los anticuerpos, se administran tratamientos inmunosupresores. En 2021 se aprobó en España el uso de caplacizumab. Es un anticuerpo que actúa evitando la unión del factor von Willebrand a las plaquetas, disminuyendo su agregación y el riesgo de desarrollar microtrombosis. Este fármaco ha mejorado la supervivencia y evolución de los pacientes. Se utiliza de forma combinada con el recambio plasmático y con inmunosupresores.
En resumen, la púrpura trombótica trombocitopénica es una enfermedad hematológica rara, englobada dentro de los síndromes micorangiopáticos, que cursa con anemia, esquistocitos y trombocitopenia. Es una enfermedad grave y de curso fatal si no se inicia el tratamiento de forma urgente.
Dra. Begoña Pérez de Camino.
Servicio de Hematología y Hemoterapia
Hospital Universitario Fundación Jiménez Díaz
- 202327ene
Trombocitopenia inmune o PTI, aspectos importantes que debemos conocer
Las siglas PTI corresponden a trombocitopenia inmune, una enfermedad autoinmune que se caracteriza por una cifra baja de plaquetas disminuidas (<100 x109/L). Es una enfermedad rara que afecta a hombres y mujeres de todas las edades; con una incidencia de 2-5 casos por 100.000 cada año.
Aclaremos en primer lugar; ¿qué son las plaquetas? Son células sanguíneas que ayudan a evitar el sangrado tras una lesión. En general, los recuentos de plaquetas oscilan entre 150 y 450 x109/L.
En los pacientes con PTI, el sistema inmunitario ataca y destruye las propias plaquetas. Además, impide su correcta producción en la médula ósea. Como resultado, el número de plaquetas circulantes es más bajo de lo normal. Esto hace que aumente el riesgo de sangrado, especialmente cuando el recuento de plaquetas es <20-30 x109/L.
Y, ¿cuál es la causa de este ataque por parte de nuestro propio sistema inmune? En la mayoría de los casos, la causa que desencadena la PTI es desconocida, aunque puede deberse a: infecciones, enfermedades autoinmunes, inmunodeficiencias, embarazo, medicamentos, productos de herbolario, vacunaciones...
¿Qué síntomas tienen los pacientes con PTI?
Cada paciente es diferente y la PTI se puede presentar de forma muy variable. Los síntomas más frecuentes son: cansancio, hematomas (moratones) y/o petequias (pequeñas manchas rojas o violáceas puntiformes en la piel), sangrado de encías (gingivorragia) y/o ampollas de color oscuro en la boca, sangrado de nariz (epistaxis), sangrado digestivo, menstruación abundante….
Los síntomas menos frecuentes incluyen sangrados a otros niveles (en las heces, en la orina, a nivel ocular o a nivel cerebral) y también trombosis, ocluyendo el flujo de sangre a través de un vaso sanguíneo.
El diagnóstico se basa en una historia clínica detallada, exploración física y análisis de sangre que incluya frotis sanguíneo (visualización de la sangre en el microscopio), estudio de infecciones víricas, enfermedades autoinmunes... En ocasiones, se tendrá que ampliar el estudio con otras pruebas como el estudio medular (aspirado o biopsia de médula ósea).
El tratamiento de la PTI debe ser individualizado, dependiendo no sólo de la cifra de plaquetas sino también de las manifestaciones hemorrágicas, las enfermedades asociadas y la necesidad de realizar procedimientos invasivos. De hecho, no todos los pacientes con PTI van a necesitar tratamiento al diagnóstico. El objetivo es conseguir una cifra de plaquetas suficiente (en general, más de 30 x109/L) para prevenir los sangrados con el menor número de efectos secundarios.
El tratamiento inicial se basa actualmente en corticoides y/o inmunoglobulinas. En caso de que no haya respuesta o suceda una recaída, pueden emplearse agonistas del receptor de la trombopoyetina, fostamatinib, fármacos anti-CD20, o realizar una esplenectomía (extirpación del bazo). Existen numerosos ensayos clínicos con fármacos prometedores que ampliarán las opciones terapéuticas en los próximos años.
La evolución de la PTI es impredecible y a menudo se hace crónica, pero en ocasiones puede resolverse de forma espontánea. Afortunadamente, los tratamientos mencionados, encaminados a incrementar el recuento de plaquetas y disminuir el riesgo de sangrado, pueden controlar la enfermedad en más del 80% de los casos, si bien también son importantes determinados cambios en el estilo de vida que pueden ayudar a mejorar la situación.
¿Qué consejos ayudan a mejorar la calidad de vida en los pacientes con PTI?
La fatiga que experimentan algunos pacientes con PTI puede llegar a afectar a la capacidad para realizar actividades cotidianas, a la concentración y a la memoria. Se trata de un síntoma especialmente frecuente en las enfermedades autoinmunes, y aunque su mecanismo no está claro, estilos de vida no saludables, los trastornos del sueño causados por algunos medicamentos y la deficiencia de hierro producida como consecuencia de los sangrados podrían relacionarse con la misma. Por ello se recomienda:
- Solicitar información sobre la enfermedad y opciones de tratamiento a su Hematólogo/a.
- Informar de sangrados relevantes que permitan evaluar periódicamente la necesidad de incrementar farmacológicamente los niveles de hierro.
- Realizar actividad física adecuada a la edad y a las condiciones físicas. Deportes y actividades que no son de contacto como yoga, natación, carrera suave, bicicleta estática, caminar o bailar, pueden ser algunas de las alternativas.
- Dormir lo suficiente y mantener un horario regular.
- Llevar una alimentación saludable, dieta equilibrada en nutrientes y horario regular.
- Reducir el estrés e incluir actividades relajantes como meditación y ejercicios de respiración.
¿Puedo realizar un viaje largo? Es una pregunta que los pacientes hacen con frecuencia. En las primeras semanas del diagnóstico de la PTI es recomendable evitar los viajes, sobre todo en avión. Posteriormente, cuando la enfermedad esté estable, podrá viajar, aunque es recomendable que siempre consulte con su Hematólogo/a para una valoración individualizada.
Además, aunque los síntomas más frecuentes están relacionados con el sangrado, es importante recordar que la PTI también conlleva un mayor riesgo de trombosis. Los vuelos o los desplazamientos por otro medio de locomoción de larga distancia (> 4 horas) son un factor de riesgo de trombosis venosa profunda, lo que se denomina "trombosis del viajero". Lo anterior, sumado a otros posibles factores como la deshidratación, el alcohol o la cafeína podrían favorecer la trombosis incluso con un recuento bajo de plaquetas.
Si tras la valoración de su hematólogo/a va a realizar un viaje es muy recomendable que: flexione los dedos de los pies, los tobillos y las rodillas mientras está sentado; camine periódicamente arriba y abajo del avión; beba mucha agua y evite el alcohol.
Dra. Nuria Revilla Calvo
Médico Adjunto del Servicio de Hematología
Miembro de la Unidad de Trombosis y Hemostasia
Hospital Universitario Fundación Jiménez Díaz
10 comentarios
Información divulgativa sobre los problemas de coagulación, prevención, diagnóstico, tipología, tratamientos y problemas asociados.
 Dra. Pilar Llamas SilleroJefe del Servicio de Hematología de la Fundación Jiménez Díaz. Directora de la Unidad de Trombosis y Hemostasia de la Fundación Jiménez Díaz.Dra. Rosa VidalMédico Adjunto del Servicio de Hematología de la Fundación Jiménez Díaz. Miembro de la Unidad de Trombosis y Hemostasia de la Fundación Jiménez Díaz.
Dra. Pilar Llamas SilleroJefe del Servicio de Hematología de la Fundación Jiménez Díaz. Directora de la Unidad de Trombosis y Hemostasia de la Fundación Jiménez Díaz.Dra. Rosa VidalMédico Adjunto del Servicio de Hematología de la Fundación Jiménez Díaz. Miembro de la Unidad de Trombosis y Hemostasia de la Fundación Jiménez Díaz.- Cuando tus defensas no funcionan como deberían: guía básica para comprender las inmunodeficiencias primarias
- Anemias hemolíticas: cuando los glóbulos rojos son destruidos antes de tiempo
- La anemia de células falciformes: Una enfermedad hereditaria de la sangre
- Transformando vidas: cómo los ensayos clínicos mejoran la supervivencia en pacientes con cáncer hematológico
- Las plaquetas: pequeñas guardianas de tu salud
La finalidad de este blog es proporcionar información de salud que, en ningún caso sustituye la consulta con su médico. Este blog está sujeto a moderación, de manera que se excluyen de él los comentarios ofensivos, publicitarios, o que no se consideren oportunos en relación con el tema que trata cada uno de los artículos.
Quirónsalud no se hace responsable de los contenidos, opiniones e imágenes que aparezcan en los "blogs". En cualquier caso, si Quirónsalud es informado de que existe cualquier contenido inapropiado o ilícito, procederá a su eliminación de forma inmediata.
Los textos, artículos y contenidos de este BLOG están sujetos y protegidos por derechos de propiedad intelectual e industrial, disponiendo Quirónsalud de los permisos necesarios para la utilización de las imágenes, fotografías, textos, diseños, animaciones y demás contenido o elementos del blog. El acceso y utilización de este Blog no confiere al Visitante ningún tipo de licencia o derecho de uso o explotación alguno, por lo que el uso, reproducción, distribución, comunicación pública, transformación o cualquier otra actividad similar o análoga, queda totalmente prohibida salvo que medie expresa autorización por escrito de Quirónsalud.
Quirónsalud se reserva la facultad de retirar o suspender temporal o definitivamente, en cualquier momento y sin necesidad de aviso previo, el acceso al Blog y/o a los contenidos del mismo a aquellos Visitantes, internautas o usuarios de internet que incumplan lo establecido en el presente Aviso, todo ello sin perjuicio del ejercicio de las acciones contra los mismos que procedan conforme a la Ley y al Derecho.